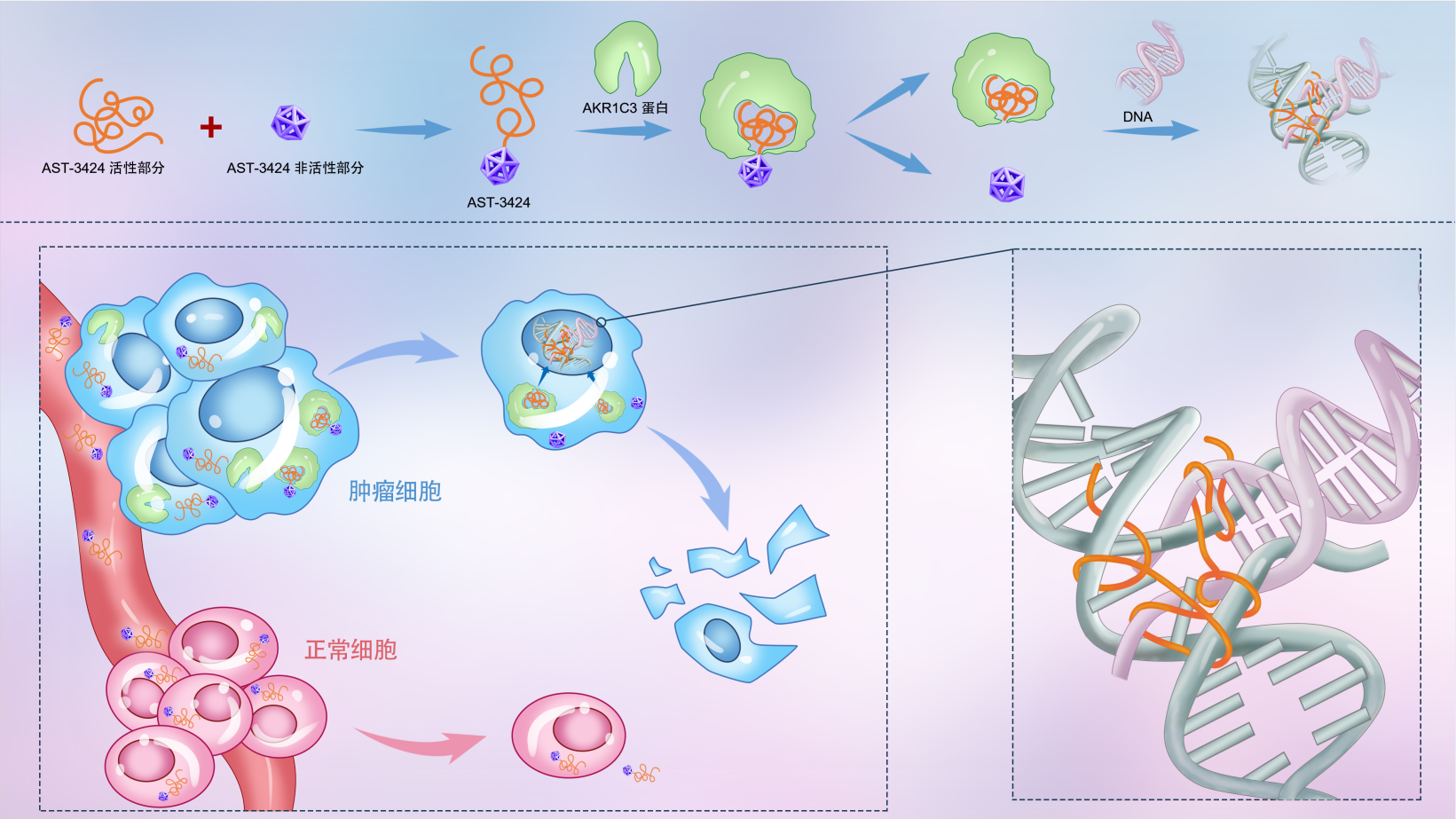
AST-3424,是由艾欣达伟研发团队全球首创(first-in-class)的依赖AKR1C3酶活化的小分子偶联靶向药物,通过醛酮还原酶家族1成员C3(AKR1C3)选择性裂解成具有细胞毒性的活性形式(AST-2660)。AST-3424释放的双氮丙啶(AST-2660)与标准化疗药物噻替派和丝裂霉素C类似,在鸟嘌呤的N7(或O6)位置使DNA烷基化并交联从而导致细胞死亡。
由美国国家癌症研究所(NCI)委托SWOG开展复发难治性T-ALL II期临床研究。
复发难治性T-ALL II期临床研究(ClinicalTrials.gov 识别号: NCT04315324)单臂、开放、OBI-3424单药(每21天一个治疗周期,第1及第8天给药)由SWOG主导开展(Southwest Oncology Group,创建于1956年,美国国家癌症研究所为主要资金赞助者。截至目前SWOG试验已获批准14种抗癌药物,改变了100多种癌症治疗标准,您可在swog.org了解更多相关信息)NIH基金号:U10CA180888。
AST-3424的亚洲区外商业权利属于公司全球合作伙伴OBI,该产品第一/二期剂量递增阶段(dose escalation)试验在美国德州大学MD安德森癌症中心(M.D. Anderson Cancer Center)及俄亥俄州立大学The James Cancer Hospital and Solove Research Institute进行,并同时进行剂量限制性毒性(dose limiting toxicity)评估。
AST-3424项目在中国的临床研究由深圳艾欣达伟医药科技有限公司独立开展。
AST-3424实体瘤Ⅰ期临床试验由上海市东方医院肿瘤医学部主任、中国临床肿瘤学会(CSCO)前任理事长李进教授主持,目前已顺利结束。AST-3424肝癌II期临床试验由中国人民解放军第八一医院副院长,全军肿瘤中心主任,国家药物临床试验机构主任秦叔逵教授主持,即将展开。
AST-3424急性T淋巴细胞白血病Ⅰb期临床试验正在哈尔滨第一医院、中国医学科学院血液病医院、北京大学第三医院入组患者,分别由马军教授、王建祥教授和景红梅教授主持研究。
1.在美国进行的T-ALL适应症的II期临床实验在2021年4月入组了第1例患者。
2.在2020年5月美国临床肿瘤学会(ASCO)在线年会上,OBI发表了相关结果论文,说明OBI-3424第一/二期临床试验进程与初步资料。
(2020 ASCO VIRTUAL ANNUAL MEETING,Abstract: TPS3658 / Poster: 388,A first-in-man phase I/II study of OBI-3424, an AKR1C3-selective bis-alkylating agent prodrug, in subjects with advanced cancer, including hepatocellular carcinoma (HCC) and castrate-resistant prostate cancer (CRPC),
OBI-3424第二期族群扩增(cohort expansion phase)试验将以免疫组织化学染色法(IHC)筛选AKR1C3酶高度表现的患者为受试对象。